Psoriasi: cos’è, caratteristiche, fattori e terapie biologiche per il trattamento
Ultima modifica: 23 Dicembre 2025
Hai bisogno di un parere su questa condizione?

Dott.ssa Annunziata Dattola
30 minuti - 65 € 15 anni di esperienza Area di Dermatologia e Venereologia Richiedi una televisita con: Dott.ssa Annunziata DattolaGarantito in 24 ore! Con questo specialista o un suo collega.
Il termine “psoriasi” deriva dal greco ψωρίασις – psōríasis e significa di “condizione di prurito”. Si tratta di una malattia antichissima. Secondo alcuni studiosi le prime descrizioni riguardanti la psoriasi sarebbero comparse addirittura nei Codici Assiro Babilonesi (intorno al 2000 a.C. circa) che descrivono malattie cutanee squamo crostose, ma anche in alcuni papiri egiziani e in diversi libri dell’Antico Testamento.
Nel nostro articolo daremo una definizione di psoriasi, ne approfondiremo le possibili cause e vedremo le principali cure e le terapie biologiche innovative a cui oggi si può ricorrere nei casi più gravi.
Per maggiori informazioni sulla psoriasi, le possibili cause, le principali cure e le terapie biologiche innovative a cui oggi si può ricorrere nei casi più gravi, puoi chiedere un consulenza a un dermatologo online cui porre tutte le domande che desideri.
Che cos’è la psoriasi e quanto è diffusa in Italia
La psoriasi è una dermatite eritemato-squamosa a decorso cronico, su base genetica, con patogenesi complessa, prevalenza immunitaria, caratterizzata da eruzioni eritomato-desquamanti a margini netti e di varia dimensione. Prevede fasi di miglioramento, di remissione spontanea e di esacerbazione. È spesso associata ad artropatia.
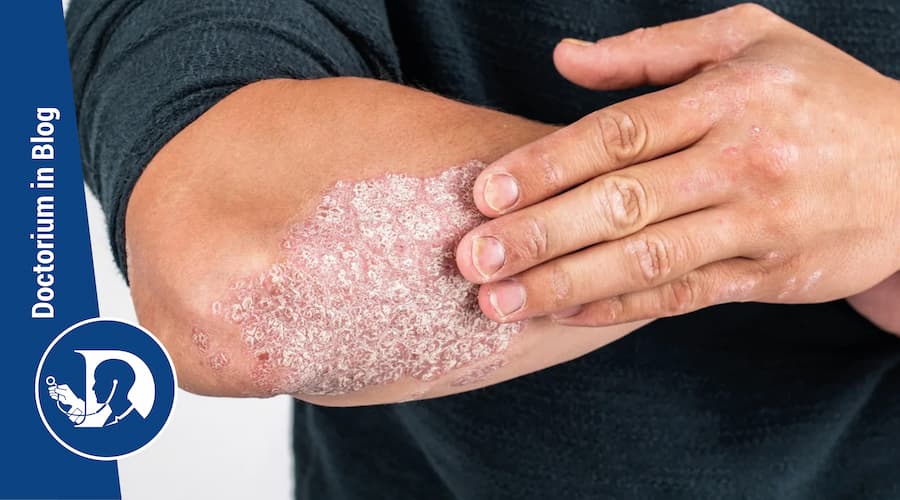
La lesione dermatologica si presenta come un alone periferico con desquamazione (squame bianco-argentee) sulla superficie definita “lesione eritemato-desquamativa”.
La prevalenza della psoriasi in Italia è del 3-4%.
Nella maggior parte dei casi si presenta in forma lieve, ma si possono manifestare anche forme più severe a cui si associano altre complicanze come ad esempio artropatie. E’ spesso associata a disturbi di carattere sistemico, tra cui la sindrome metabolica (diabete, dislipidemia, obesità) e sembra essere correlata ad un aumentato rischio di malattie cardiovascolari, tra cui ictus e infarto del miocardio.
Fattori genetici, ambientali ed immunologici
Si possono differenziare due quadri fenotipici:
- Tipo 1: <40 anni, giovanile, forte associazione con fenotipo HLA- CW6 DR7.
- Tipo 2: 60 anni, bassa familiarità, non esprime il fenotipo HLA – CW6 DR7.
Nella patogenesi coesistono sia fattori genetici che ambientali. Entrambi entrano in relazione con i fattori immunologici: il linfocita T attivato CD4+, in seguito ad espansione clonale a livello linfonodale, migra a livello della cute e ivi rilascia citochine quali TNF-α, IL-12, IL-17, IL-22, IL-23 che determineranno tutto il processo patologico: vasodilatazione, eritema, desquamazione con alterazione del turnover dei cheratinociti.
La psoriasi è una patologia di tipo complesso, caratterizzata dall’interazione tra più geni predisponenti (o loci di suscettibilità) e fattori ambientali che, insieme, determinano la predisposizione individuale o familiare a sviluppare le varie forme della patologia. La psoriasi è una malattia con una evidente componente di familiarità, dal momento che spesso insorge in individui diversi della stessa famiglia. C’è una forte concordanza tra gemelli omozigoti.
Sono stati sinora identificati 8 loci genici di suscettibilità alla psoriasi. Il più importante è il locus sul braccio corto del cromosoma 6, PSORS1. Questo locus è localizzato in una regione comprendente il complesso maggiore di istocompatibilità (MHC), in cui sono localizzati i geni per gli HLA. Questa regione è considerata il maggior locus di suscettibilità alla psoriasi ed è responsabile del 30-50% dei casi della malattia.
Cosa accade nella psoriasi
Il tratto distintivo fondamentale della malattia psoriasica è una incontrollata proliferazione dei cheratinociti (cellule della pelle), associata ad una significativa alterazione del processo di differenziamento di queste cellule. In aggiunta, linfociti (cellule guardiane) provenienti dal circolo ematico si infiltrano a livello del derma e dell’epidermide, instaurando una condizione infiammatoria a livello della lesione cutanea.
Fattori esterni, traumi, condizioni infettive determinano il richiamo dei linfociti T che migrano e rilasciano in situ citochine infiammatorie.
Dal punto di vista istopatologico avremo caratteristiche particolari: vasodilatazione del vaso terminale a livello delle papille dermiche, extravasazione di linfociti e neutrofili, infiltrato infiammatorio a livello del derma, proliferazione degli strati dell’epidermide. Fisiologicamente i cheratinociti sono sottoposti a turnover cellulare, migrano dallo strato basale a quello corneo dove perdono il nucleo. Nella psoriasi c’è un’alterazione di questo processo con presenza di cellule nucleate anche nello strato superficiale, fenomeno noto come “paracheratosi”.
Hai bisogno di un parere su questa condizione?

Dott.ssa Annunziata Dattola
30 minuti - 65 € 15 anni di esperienza Area di Dermatologia e Venereologia Richiedi una televisita con: Dott.ssa Annunziata DattolaGarantito in 24 ore! Con questo specialista o un suo collega.
Quali sono i fattori scatenanti
Poiché la psoriasi è una malattia cronica caratterizzata da periodi di remissione alternati a fasi di riacutizzazione, riconoscerne i fattori scatenanti è importante anche al fine di evitare abitudini e comportamenti che possano aggravare o indurre una ripresa della malattia.
Essi possono essere:
- Traumi: cicatrici chirurgiche, grattamento, tatuaggi (fenomeno di Koebner);
- Infezioni: esiste un’associazione molto stretta tra infezione dell’apparato oro-faringeo da Streptococco β-emolitico di gruppo A e psoriasi;
- Farmaci: beta-bloccanti, in quanto molte volte la psoriasi insorge in pazienti ipertesi che sono in trattamento con beta-bloccanti. Altri farmaci precipitanti sono i sali di litio, ace-inibitori, antimalarici, IFN alfa, tetracicline, FANS;
- Fattori endocrini: ipocalcemia, periodo mestruale, pubertà, menopausa, estrogeni ad alte dosi, ipercolesterolemia, sindrome metabolica;
- Fattori ambientali: le radiazione UV vengono usate per curare la psoriasi per il loro effetto immunomodulante perché regolano il turn over dei cheratinociti e bloccano l’infiammazione alla base della patologia. Se però si sviluppa un eritema solare non si ha nessun effetto benefico anzi rappresenta un fattore stressogeno importante;
- Stress psicofisico;
- Immunodeficienza (HIV);
- Alcool, fumo.
Varianti cliniche
- Psoriasi Volgare
- A placche (più frequente)
- Ungueale
- Intertriginosa o delle pieghe
- Della mucosa (rara)
- P. guttata (a gocce; se le papule sono più grandi si definisce P. Nummulata)
- P. pustolosa (pustola amicrobica, sterile determinata da stravaso di neutrofili)
- Localizzata
- Generalizzata
- P. eritrodermica (più grave)
- P. artropatica o Artrite Psoriasica
Terapia
La terapia si divide in:
- Terapia topica (creme e pomate);
- Fototerapia (effetto immunomodulante naturale della luce);
- Terapia sistemica: metotrexato, ciclosporina A, retinoidi e farmaci biologici.
Farmaci biologici utilizzati per il trattamento della psoriasi
Il primo anticorpo monoclonale utilizzato in dermatologia, per il trattamento della psoriasi, è stato l’Infliximab (nome commerciale Remicade®).
La sua approvazione da parte della FDA risale all’agosto del 1998.
Dopo questa data i farmaci biologici hanno acquisito sempre maggiore importanza per il trattamento delle varie forme di psoriasi.
Attualmente, oltre all’Infliximab, in dermatologia la terapia biologica si avvale di altri farmaci come Adalimumab (nome commerciale Humira®), Etanercept (nome commerciale Enbrel®), Ustekinumab (nome commerciale Stelara®), Golimumab (nome commerciale Simponi®), Secukinumab (nome commerciale Cosentyx®).
Questi farmaci, eccetto Ustekinumab, interferiscono con l’azione del TNF- α. Elevati livelli della molecola sopra citata sono stati trovati nella sinovia e nelle placche psoriasiche di pazienti con artrite psoriasica e nel siero e nel tessuto sinoviale di pazienti con spondilite anchilosante. Nella psoriasi a placche, l’infiltrazione di cellule infiammatorie, comprese le cellule T, porta ad un aumento dei livelli di TNF nelle lesioni psoriasiche rispetto ai livelli presenti nella cute non affetta. Vediamoli ora uno per uno.
Infliximab (Remicade®)
L’infliximab è un anticorpo monoclonale chimerico che si lega con alta specificità e affinità sia alla forma solubile sia a quella trans-membrana del Tumor Necrosis Factor (TNF-alfa), inibendone l’attività. L’infliximab pertanto agisce riducendo l’infiammazione e l’iperproliferazione rispettivamente dell’eritema e della formazione della squama. Attualmente in Italia è stato approvato nella terapia dell’artrite reumatoide, della malattia di Crohn, della spondilite anchilosante, per l’artrite psoriasica e per la psoriasi. La somministrazione del farmaco avviene per via endovenosa.
Adalimumab (Humira®)
Adalimumab è l’anticorpo monoclonale umano che blocca l’azione del TNF-alfa. Si lega selettivamente a quest’ultimo e ne neutralizza la sua funzione biologica. Blocca la sua interazione con i recettori del TNF-alfa di membrana cellulare, p55 e p75.
Adalimumab modula anche le risposte biologiche che sono indotte o regolate dal TNF-alfa, inclusi i cambiamenti dei livelli delle molecole di adesione responsabili della migrazione dei leucociti (ELAM-1, VCAM-1, e ICAM-1); viene utilizzato in dermatologia per il trattamento dell’artrite psoriasica e nelle psoriasi a placche nei pazienti che non hanno risposto o che presentano controindicazioni alle terapie sistemiche con metotrexato, ciclosporina o PUVA.
La dose raccomandata per i pazienti affetti da artrite psoriasica è di 40 mg di Adalimumab somministrati ogni due settimane in dose singola per via sottocutanea. I dati disponibili suggeriscono che la risposta clinica viene solitamente ottenuta entro 12 settimane dall’inizio del trattamento. Nei casi di mancata risposta entro questo periodo di tempo, la continuazione della terapia deve essere valutata con particolare attenzione.
Nei pazienti che entro questo periodo di tempo non hanno sviluppato una risposta soddisfacente, sarebbe opportuno valutare attentamente se sia il caso di proseguire la terapia oltre le 16 settimane.
Da trial clinici condotti confrontando Adalimumab con il placebo e metotrexato è stato evidenziato come pazienti trattati con Adalimumab mostravano miglioramenti significativi.
Etanercept (Enbrel®)
L’Etanercept è una proteina di fusione ottenuta tramite tecniche di DNA ricombinante del recettore umano p75 del fattore TNF-alfa con la frazione Fc dell’immunoglobulina umana IgG1.
La proteina funziona da recettore solubile per il TNF-alfa e possiede un’affinità di legame per il TNF-alfa più alta di quella degli altri recettori del corpo umano che si lega al TNFα andando ad inibire la sua attività nel processo evolutivo dell’infiammazione, sia nell’uomo sia negli animali.
Si pensa che il meccanismo d’azione dell’etanercept consista in una inibizione competitiva del legame del TNF ai recettori superficiali TNFR, che previene le risposte cellulari mediate dal TNF rendendo il TNF biologicamente inattivo.
Enbrel è disponibile in dosaggi da 10, 25 e 50 mg.
Nell’Artrite Psoriasica, la dose raccomandata è di 25 mg di Etanercept somministrati due volte a settimana, o 50 mg somministrati una volta alla settimana.
I dati disponibili suggeriscono che di solito si ottiene una risposta clinica entro 12 settimane dall’inizio del trattamento. In un paziente che non risponde entro questo periodo di tempo, il proseguimento della terapia deve essere attentamente riconsiderato.
Nella psoriasi pediatrica la dose raccomandata è di 0,8mg/kg una volta a settimana per 24 settimane, non è raccomandato in una popolazione di età inferiore ai 6 anni.
Diversi trial, tra i pazienti con psoriasi a placche che hanno ricevuto il trattamento con Etanercept, hanno evidenziato risposte significative rispetto al placebo al momento della prima visita (2 settimane) e si sono mantenute per le 24 settimane di terapia. Etanercept è stato significativamente migliore rispetto al placebo per tutti gli indici di attività della malattia (p < 0,001), e le risposte sono state simili con o senza una terapia concomitante con metotrexato.
Ustekinumab (Stelara®)
Ustekinumab è un anticorpo monoclonale IgG1κ interamente umano, che lega interleuchina (IL)- 12/23, prodotto in una linea cellulare di mieloma murino, usando la tecnologia di DNA ricombinante, Ustekinumab lega con specificità la proteina p40, sub-unità condivisa delle interleuchine (IL)-12 e IL-23, citochine umane. Inibisce l’attività biologica di IL-12 e di IL-23 umane, impedendo il legame di p40 con la proteina recettoriale IL-12R1 espressa sulla superficie delle cellule immunitarie. Ustekinumab non può legarsi a IL-12 o a IL-23 che sono già legate ai recettori IL-12R1 presenti sulla superficie cellulare.
IL-12 e IL-23 sono citochine secrete da cellule attivate presentanti l’antigene, come macrofagi e cellule dendritiche ed entrambe le citochine partecipano all’attività immunitaria; IL-12 stimola le cellule natural killer (NK) e conduce la differenziazione delle cellule T CD4+ verso il fenotipo T helper 1 (Th1), IL-23 induce il pathway del T helper 17 (Th17). Tuttavia, la regolazione anomala di IL-12 e IL-23 è stata associata a patologie immuno-mediate, come la psoriasi e l’artrite psoriasica.
Ustekinumab in dermatologia è indicato per il trattamento della psoriasi a placche e per l’artrite psoriasica in pazienti che non hanno risposto o che presentano controindicazioni al trattamento sistemico con ciclosporina, metotrexato e farmaci antireumatici modificanti la malattia non biologici (DMARDs).
La posologia raccomandata di Ustekinumab è una dose iniziale di 45 mg somministrata per via sottocutanea, seguita da una dose di 45 mg dopo 4 settimane e, successivamente, ogni 12 settimane.
Occorre prendere in considerazione l’interruzione del trattamento nei pazienti che non hanno mostrato alcuna risposta ad un trattamento di 28 settimane.
Golimumab (Simponi®)
Golimumab è un anticorpo monoclonale umano che forma complessi stabili ad elevata affinità sia per la forma solubile, sia per quella transmembrana bioattiva del TNF-α umano, impedendo il legame del TNF-α ai suoi recettori. Il legame di golimumab al TNF alfa umano ha mostrato di inibire l’espressione sulla superficie cellulare delle molecole di adesione, selettina E, molecola di adesione alle cellule vascolari di tipo 1 (VCAM) e molecola di adesione intracellulare di tipo 1 (ICAM) da parte delle cellule endoteliali umane. In vitro inibisce la secrezione del TNF alfa da parte delle cellule endoteliali indotta da IL-6, IL8 e GM-CSF.
In dermatologia, somministrato singolarmente o in associazione con il metotrexato, è indicato per il trattamento dell’artrite psoriasica in fase attiva e progressiva, negli adulti, qualora sia stata inadeguata la risposta a precedenti trattamenti DMARD. Golimumab ha dimostrato di ridurre il tasso di progressione del danno articolare periferico, misurato con i raggi X in pazienti con sottotipi di malattia poliarticolare simmetrica.
La somministrazione prevede una dose di 50 mg una volta al mese, nello stesso giorno di ogni mese. I dati clinici evidenziano che la risposta clinica si ottiene dopo 12-14 settimane dall’inizio del trattamento, per i pazienti che non traggono beneficio dal trattamento è necessario valutare se continuare la terapia con il suddetto farmaco.
L’efficacia e la sicurezza di Golimumab sono state valutate in uno studio clinico multicentrico, randomizzato, in doppio cieco, controllato con placebo (GO-REVEAL study), condotto in 405 pazienti adulti con AP in fase attiva (≥ 3 articolazioni tumefatte e ≥ 3 articolazioni dolenti), nonostante la terapia con antinfiammatori non steroidei (FANS) o DMARD.
Alla settimana 24, nei pazienti trattati con Golimumab, sono stati osservati miglioramenti nei parametri dell’attività periferica tipica dell’artrite psoriasica (ad esempio, numero di articolazioni tumefatte, numero di articolazioni dolenti, dattilite e entesite).
Hai bisogno di un parere su questa condizione?

Dott.ssa Annunziata Dattola
30 minuti - 65 € 15 anni di esperienza Area di Dermatologia e Venereologia Richiedi una televisita con: Dott.ssa Annunziata DattolaGarantito in 24 ore! Con questo specialista o un suo collega.
Bibliografia
- Shai, D. Vardy et al., Psoriasis, biblical afflictions and patients’ dignity, in Harefuah, 2002;
- Rachakonda TD et al., Psoriasis prevalence among adults in the United States. J Am Acad Dermatol. 2014; 70: 512–16.
- Ghazizadeh, M. et al., Clinical improvement in psoriasis with treatment of associated hyperlipidemia, in Am J Med Sci, 2011;
- Nickoloff, The immunologic and genetic basis of psoriasis, Arch Dermatol, 1999;
- Krueger GG et al. A human interleukin12/23 monoclonal antibody for the treatment of psoriasis. N Engl J Med. 2007; 356:580–92.
- Diani M et al., T cell responses in psoriasis and psoriatic arthritis, in Autoimmun Rev, 2015;
- Liu J.K.H ”The history of monoclonal antibody development. Progress, remaining challenges and future innovations”. Annals of Medicine and Surgery 2014;
- Saurat JH et al. Efficacy and safety results from the randomized controlled comparative study of adalimumab vs. methotrexate vs. placebo in patients with psoriasis (CHAMPION), Br J Dermatol. 2008;
- Leonardi CL et al. Etanercept as monotherapy in patients with psoriasis. N Engl J Med. 2003;
- Ghazizadeh, et al., Clinical improvement in psoriasis with treatment of associated hyperlipidemia, Am J Med Sci, 2011;
- Lernia V et al., Impact of body mass index on retention rates of anti-TNF-alfa drugs in daily practice for psoriasis, J Dermatolog Treat, 2012;
- Sohini M, et al., Golimumab mAbs Epub, 2009.
Categorie
- Allergie e intolleranze
- Apparato Urogenitale
- Autismo e Disturbi dello Spettro Autistico
- Benessere Psichico e Salute mentale
- Caduta dei Capelli
- Coronavirus
- Disfunzioni della Tiroide
- Disturbi Alimentari
- Disturbi del Sonno
- Disturbi Gastrointestinali
- Epidemie e pandemie
- Farmaci - Terapie - effetti collaterali
- Malattie Autoimmuni
- Malattie infettive
- Malattie Infiammatorie
- malattie renali
- Malattie Respiratorie
- Malattie Reumatiche
- News
- Patologie Cardiovascolari
- Patologie del Piede
- Patologie del Sangue e della Coagulazione
- Patologie del Sistema Nervoso
- Patologie della Pelle
- Patologie Oculari
- Prevenzione e salute
- Problemi Muscoloscheletrici
- Salute dei Bambini
- Salute dell'Anziano
- Salute della Donna
- Sessualità e coppia
- Telemedicina
- Terapie e Rimedi Naturali
- Terapie Oncologiche
- Viaggi e Salute
- Video
- Vivere con il Diabete






