Dupilumab: la terapia biologica per la dermatite atopica moderata e grave
Ultima modifica: 30 Novembre 2024
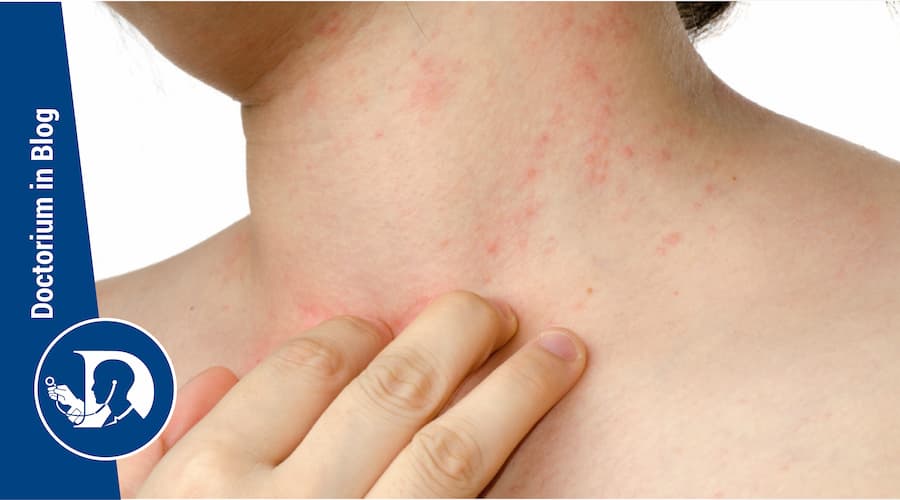
La dermatite atopica è una malattia infiammatoria cronica della pelle caratterizzata da lesioni pruriginose, eritematose e desquamanti. È responsabile di un importante peggioramento della qualità della vita di chi ne è affetto ed ha un impatto economico significativo.
I pazienti affetti da dermatite atopica sono maggiormente esposti al rischio di contrarre infezioni della pelle con conseguenze sistemiche e maggiori ospedalizzazioni.
Se ti è stata diagnosticata la dermatite atopica o hai notato lesioni sulla pelle che causa prurito, puoi chiedere un consulenza a un dermatologo online a cui porre tutte le domande che desideri.
Registrati su Doctorium e chiedi un consulto.
Cosa provoca la comparsa della dermatite atopica?
L’eziologia della dermatite atopica è multifattoriale. Esiste un’interazione tra i fattori genetici, la funzione di barriera cutanea, la disregolazione immunitaria e la microflora cutanea. Non è tuttavia ancora noto se l’infiammazione cutanea derivi inizialmente dai difetti strutturali della barriera epidermica o dalla disregolazione immunitaria.
Studi recenti hanno fornito ulteriori informazioni sui fattori immunologici alla base della patogenesi della dermatite atopica. Si è visto che la dermatite atopica è una malattia prevalentemente dominata da linfociti T Helper di tipo 2, con ruoli aggiuntivi da parte di citochine in alcuni sottotipi di malattia. Le analisi cellulari e molecolari delle lesioni acute e croniche hanno dimostrato un aumento progressivo dell’espressione genica relativa a TH2, TH22 e geni codificanti citochine, con attivazione simultanea della risposta infiammatoria associata a TH1. È stato anche dimostrato che gli infiltrati di cellule linfoidi innate di tipo 2 nelle lesioni promuovono risposte da parte dei TH2 inducendo la produzione di citochine associate ai TH2 come l’interleuchina IL-4 e IL-13.
Il ruolo dell’Interleuchina 4 e 13 (IL-4, IL-13)
IL-4 e IL-13 svolgono un ruolo importante nella risposta infiammatoria mediata dai TH2 che si riscontra nella dermatite atopica.
In particolare l’IL-4 guida la differenziazione delle cellule TH2 e la commutazione di classe delle IgE nei linfociti B.
L’IL-13 viene prodotta dalle cellule TH2. E’ coinvolta nella maturazione e differenziazione delle cellule B e nella chemiotassi degli eosinofili ed è un mediatore centrale dell’asma allergico. Queste citochine inoltre provocano la sottoregolazione dell’espressione dei geni coinvolti nella funzione e nell’integrità della barriera cutanea. La sovraespressione di IL-4 e IL-13 nella dermatite atopica previene la sovraregolazione dei peptidi antimicrobici in risposta a stimoli batterici e virali nella pelle. Ciò contribuisce ulteriormente ai difetti di barriera ed esacerba l’infiammazione, esponendo il paziente a un aumentato rischio di infezione da Staphylococcus aureus.
La terapia classica
Il trattamento attuale è incentrato su agenti topici immunomodulatori aspecifici come i corticosteroidi e gli inibitori della calcineurina per prevenire le riacutizzazioni e migliorare la funzione epidermica. Nei pazienti con dermatite atopica da moderata a grave che hanno frequenti riacutizzazioni, la terapia topica non è sufficiente per controllare adeguatamente la malattia. In questi pazienti, le opzioni di seconda linea erano limitate fino a poco tempo fa agli immunosoppressori e alla fototerapia con luce ultravioletta. La fototerapia però richiede molto tempo e non è sempre facilmente accessibile, mentre i glucocorticoidi orali, la ciclosporina e altri immunosoppressori hanno effetti collaterali a lungo termine e tossicità che ne limitano l’uso.
Dupilumab
Oggi l’immunopatogenesi della dermatite atopica è stata delineata meglio e ciò ci fornisce bersagli biologici più specifici per la terapia. L’obiettivo è quello di migliorarne l’efficacia e di ridurre al minimo gli effetti avversi.
Nel marzo 2017, la Food and Drug Association (FDA) degli Stati Uniti ha approvato “dupilumab” per il trattamento di adulti affetti da dermatite atopica moderata e grave che non è adeguatamente controllata dalle terapie topiche, successivamente è stata approvata anche in Europa. Dupilumab è un anticorpo IgG4 monoclonale completamente umano che si lega alla subunità alfa condivisa del recettore IL-4 e quindi inibisce la trasduzione del segnale di IL-4 e IL-13.
Queste citochine sono prodotte principalmente dalle cellule TH2 e hanno un ruolo centrale nella patogenesi della dermatite atopica e di altre malattie di natura atopica come per esempio l’asma, infatti dupilumab ha mostrato per la prima volta il suo effetto terapeutico proprio nei pazienti con asma da moderato a grave.
È stato osservato che dupilumab riduce significativamente i livelli sierici di chemochine attivate. Nei pazienti trattati con dupilumab, l’analisi genomica dei tessuti ha mostrato una significativa sottoregolazione dei marcatori associati all’attivazione dei linfociti T, degli eosinofili e anche dei geni correlati all’iperplasia epidermica. È stata inoltre dimostrata la sovraregolazione dei geni funzionali correlati alla barriera.
Formulazione e dosaggio di Dupilumab
Dupilumab viene somministrato per via sottocutanea. Le iniezioni possono essere somministrate da un operatore sanitario o da un caregiver o possono essere auto-somministrate. Si effettua una dose di carico iniziale di 600 mg seguita da iniezioni di 300 mg ogni settimana oppure ogni due settimane. Sono state dimostrate sicurezza ed efficacia entro un periodo di trattamento di 16 settimane degli studi di Fase III. Sono stati osservati anche miglioramenti significativi per quanto riguarda la qualità della vita, il sonno, l’ansia, e la depressione.
Effetti collaterali
I risultati di sicurezza negli studi clinici di dupilumab sono stati valutati in base all’incidenza, al tipo e alla gravità degli eventi avversi, alle indagini di laboratorio, ai segni vitali e all’elettrocardiografia.
Negli studi di fase iniziale, gli eventi avversi sono stati lievi/moderati e sono stati complessivamente simili in frequenza tra gruppi placebo e in trattamento. Inoltre sembravano essere di natura transitoria. Gli eventi avversi comuni più frequentemente osservati nei soggetti trattati con dupilumab sono stati rinofaringite, cefalea e reazioni al sito di iniezione.
Eventi avversi gravi sono stati osservati più comunemente nei gruppi placebo, comprese infezioni cutanee ed esacerbazione della dermatite atopica. I dati relativi alle infezioni cutanee hanno mostrato 0,05 infezioni per paziente nel gruppo di trattamento rispetto a 0,20 infezioni per paziente nel gruppo placebo. Ciò sottolinea ancora di più come i pazienti affetti da dermatite atopica abbiano un maggior rischio di contrarre infezioni cutanee batteriche, virali e fungine. Ciò suggerisce che, se non trattata, la mancanza di funzione di barriera cutanea nella dermatite atopica può rendere i pazienti suscettibili ad una maggiore incidenza di infezioni cutanee.
Risultati di sicurezza simili sono stati osservati nello studio di Fase IIb. Gli effetti collaterali comuni nel gruppo dupilumab includevano nasofaringite, cefalea e infezioni del tratto respiratorio superiore. Inoltre, i partecipanti trattati con dupilumab hanno sperimentato tassi più elevati di congiuntivite rispetto al placebo (7 vs 3%). Gli eventi avversi gravi sono stati riportati più frequentemente nel gruppo placebo (7 vs 4%).
Negli studi di Fase III le reazioni al sito di iniezione sono state riportate più comunemente nei gruppi di trattamento. Gli eventi avversi sono stati generalmente da lievi a moderati. Sono stati osservati tassi più elevati di congiuntivite nei gruppi di trattamento con dupilumab rispetto ai gruppi placebo. È interessante notare che non vi è alcun rapporto di aumento dell’incidenza di congiuntivite quando dupilumab è stato testato in pazienti con asma e poliposi nasale. Pertanto, la patogenesi della congiuntivite potrebbe non essere associata a dupilumab ma può essere un fattore di patogenesi della dermatite atopica stessa.
Coerentemente con gli studi precedenti, infezioni cutanee ed esacerbazioni della dermatite atopica sono state osservate più frequentemente nei gruppi placebo. Tutto ciò suggerisce un miglioramento della funzione di barriera cutanea negli individui trattati con dupilumab.
Inoltre l’8% dei soggetti nel gruppo placebo ha dovuto assumere una terapia di salvataggio con corticosteroidi sistemici rispetto al 2% dei soggetti che ricevevano dupilumab settimanalmente e all’1% dei soggetti che ricevevano iniezioni bisettimanali. In un altro studio il 13% dei soggetti nel gruppo placebo ha ricevuto la terapia di salvataggio con corticosteroidi sistemici e solo il 3 e l’1% dei soggetti negli altri due rispettivi regimi di dosaggio di dupilumab. Questi risultati supportano ulteriormente il fatto che dupilumab può ridurre la necessità per i corticosteroidi sistemici e il peso dei loro effetti collaterali.
Indicazioni cliniche
Dupilumab è stato approvato per l’uso nella gestione della dermatite atopica moderata/grave e refrattaria dell’adulto. Dupilumab può essere utilizzato in combinazione con o senza corticosteroidi topici. Gli inibitori topici della calcineurina possono essere utilizzati anche in aree come viso, collo, aree intertriginose e genitali. L’impiego del farmaco nei bambini è in corso di studi, ad oggi la sua efficacia e sicurezza nei bambini di età inferiore ai 12 anni non state ancora valutate da alcuna autorità regolatoria.
Direzioni future
Poiché la dermatite atopica è una condizione cronica le indagini future dovrebbero essere volte ad esaminare cosa accade nei pazienti che interrompono, sospendono e poi reintroducono il trattamento. Devono ancora essere effettuati studi che valutino possibili effetti di astinenza. Si deve ancora studiare se l’interruzione del farmaco comporterà o no una riacutizzazione della malattia per effetto rimbalzo o una sua esacerbazione.
Oggi si stanno studiando altri agenti biologici che hanno come obiettivo la produzione di altre citochine Th2. Una recente meta-analisi ha valutato le prove alla base dell’efficacia e della sicurezza di questi farmaci biologici in pazienti con dermatite atopica da moderata a grave. Abbiamo lebrikizumab e tralokinumab che sono anticorpi monoclonali contro IL-13. In uno studio di fase II, le iniezioni mensili di lebrikizumab con l’uso concomitante di corticosteroidi topici per 12 settimane hanno prodotto buoni risultati rispetto al placebo.
Concludiamo il nostro articolo affermando che ad oggi l’unico agente biologico che ha mostrato risultati coerenti di efficacia e sicurezza è il Dupilumab.
Hai bisogno di un parere su questa condizione?

Dott.ssa Annunziata Dattola
30 minuti - 65 € 15 anni di esperienza Area di Dermatologia e Venereologia Richiedi una televisita con: Dott.ssa Annunziata DattolaGarantito in 24 ore! Con questo specialista o un suo collega.
Bibliografia
Categorie
- Allergie e intolleranze
- Apparato Urogenitale
- Autismo e Disturbi dello Spettro Autistico
- Benessere Psichico e Salute mentale
- Caduta dei Capelli
- Coronavirus
- Disfunzioni della Tiroide
- Disturbi Alimentari
- Disturbi del Sonno
- Disturbi Gastrointestinali
- Epidemie e pandemie
- Farmaci - Terapie - effetti collaterali
- Malattie Autoimmuni
- Malattie infettive
- Malattie Infiammatorie
- malattie renali
- Malattie Respiratorie
- Malattie Reumatiche
- News
- Patologie Cardiovascolari
- Patologie del Piede
- Patologie del Sangue e della Coagulazione
- Patologie del Sistema Nervoso
- Patologie della Pelle
- Patologie Oculari
- Prevenzione e salute
- Problemi Muscoloscheletrici
- Salute dei Bambini
- Salute dell'Anziano
- Salute della Donna
- Sessualità e coppia
- Telemedicina
- Terapie e Rimedi Naturali
- Terapie Oncologiche
- Viaggi e Salute
- Video
- Vivere con il Diabete






