Cause, diagnosi e trattamento della polmonite in adulti e bambini
Ultima modifica: 20 Febbraio 2026
Hai bisogno di un parere su questa condizione?

Dott.ssa Carmela Cilione
30 minuti - 75 € 33 anni di esperienza Area di Pneumologia Richiedi una televisita con: Dott.ssa Carmela CilioneGarantito in 24 ore! Con questo specialista o un suo collega.
Cos’è la polmonite
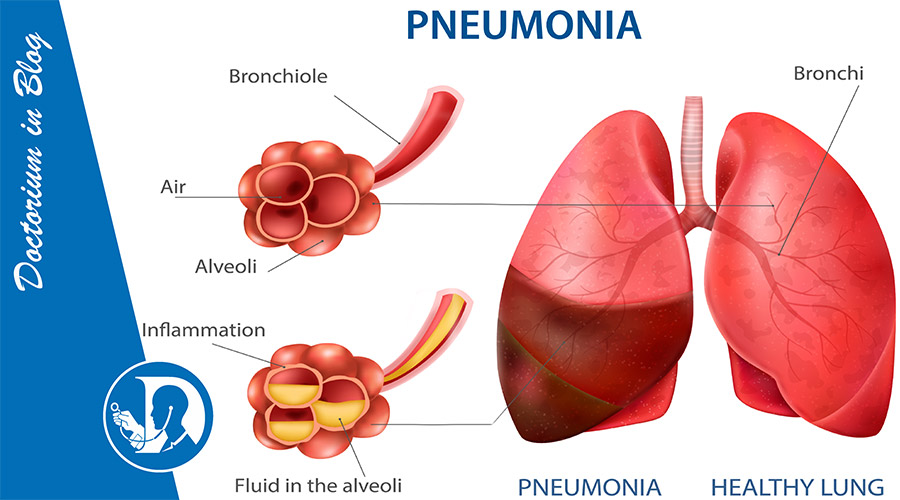
La polmonite è un’infiammazione del tessuto polmonare causata nella maggior parte dei casi da batteri, virus o, più raramente, funghi. L’infezione raggiunge gli alveoli — le piccole “sacche” d’aria all’interno dei polmoni — che si riempiono di essudato (liquido infiammatorio) e non riescono più a svolgere correttamente lo scambio di ossigeno e anidride carbonica.
Questo processo determina i sintomi tipici: febbre, tosse, fiato corto e senso di oppressione o dolore toracico. A seconda del tipo di agente causale, dell’estensione e delle condizioni generali della persona, la polmonite può presentarsi in forme lievi o molto gravi, fino a richiedere il ricovero in terapia intensiva.
La polmonite è una delle infezioni respiratorie più comuni e può colpire persone di tutte le età. È particolarmente rilevante nei bambini piccoli, negli anziani e nei pazienti con patologie croniche o difese immunitarie ridotte, nei quali il rischio di complicanze è maggiore.
Cause e fattori di rischio della polmonite
La polmonite è più spesso causata da microrganismi (batteri, virus, funghi) che raggiungono il polmone attraverso le vie respiratorie. Tuttavia, non tutti sviluppano la malattia allo stesso modo: alcuni fattori possono aumentare il rischio di ammalarsi o di sviluppare forme più gravi.
Cause infettive: batteri, virus e funghi
Sebbene l’identificazione di un agente eziologico per la polmonite sia essenziale per un trattamento efficace e per la tenuta dei registri epidemiologici, ciò è raramente riscontrato nella pratica clinica. In altre parole, anche con esami mirati non sempre è possibile individuare con certezza il germe responsabile.
Vediamo comunque gli agenti patogeni responsabili in base ai vari tipi di polmonite.
Polmonite acquisita in comunità – Cause batteriche
Sono stati classicamente studiati sotto le sottovoci organismi “tipici” e “atipici” in termini di facilità di positività colturale. I microrganismi tipici comuni includono Pneumococcus, Haemophilus influenzae, Moraxella catarrhalis, Streptococcus di gruppo A e altri organismi aerobi e anaerobi Gram-negativi.
Organismi atipici comunemente osservati nella pratica clinica includono Legionella, Mycoplasma, Chlamydia.
Polmonite acquisita in comunità – Cause virali
Spesso sono responsabili le specie virali che colonizzano il rinofaringe. È ancora da indagare se siano la causa primaria o se contribuiscano alla patogenesi da cause batteriche secondarie. Tuttavia, alcuni degli agenti virali più frequenti implicati nella CAP includono il virus dell’influenza seguito dal virus respiratorio sinciziale, dal virus della parainfluenza e dagli adenovirus. E ovviamente recentemente dal virus SARS COV-2 responsabile del COVID-19.
Polmonite acquisita in comunità – Cause fungine
Le infezioni fungine si verificano solitamente nei pazienti immunocompromessi per esempio nelle persone affette da HIV e i riceventi di trapianto di organi. Tuttavia, alcune specie fungine possono causare polmonite in individui immunocompetenti a cui si pone diagnosi tardivamente e portano a esiti sfavorevoli. I 3 più comuni includono Histoplasma, Blastomyces e Coccidioides.
Polmonite acquisita in ospedale e polmonite associata al ventilatore
Esiste una notevole sovrapposizione tra gli agenti eziologici nei pazienti ospedalizzati non ventilati e nei pazienti ventilati con polmonite ed è quindi opportuno considerarli insieme.
Non tutte le persone esposte agli stessi microrganismi sviluppano una polmonite. Alcune condizioni aumentano il rischio di ammalarsi o di incorrere in forme più severe:
- età avanzata (oltre i 65 anni) o età molto giovane (bambini sotto i 2 anni);
- presenza di malattie croniche (BPCO, asma, scompenso cardiaco, diabete, malattie renali o epatiche);
- difese immunitarie ridotte (immunodeficienze primitive o acquisite, terapie immunosoppressive, HIV);
- storia di asplenia funzionale o anatomica;
- fumo di sigaretta, abuso di alcol, malnutrizione;
- ricovero ospedaliero recente o permanenza in strutture residenziali;
- ventilazione meccanica o procedure che aumentano il rischio di aspirazione (per esempio disturbi della deglutizione);
- malattie che compromettono la clearance delle secrezioni bronchiali (per esempio fibrosi cistica, ostruzione bronchiale).
Esiste un intricato equilibrio tra gli organismi che risiedono nel tratto respiratorio inferiore e i meccanismi di difesa locali e sistemici (sia innati che acquisiti) che, quando disturbati, danno luogo all’infiammazione del parenchima polmonare, cioè la polmonite. I meccanismi di difesa comuni che sono compromessi nella patogenesi della polmonite includono:
- Alterazione dei meccanismi di difesa sistemica c che è compromessa in malattie come l’immunodeficienza comune variabile (CVID), l’agammaglobulinemia legata all’X (ereditata) e l’asplenia funzionale (acquisita).
L’immunità cellulo-mediata compromessa predispone gli individui all’infezione da organismi intracellulari come virus e organismi a bassa virulenza come la polmonite da Pneumocystis (PJP) e cause fungine; - La clearance mucociliare (sistema di pulizia delle nostre vie respiratorie) è spesso compromessa nei fumatori di sigarette, nello stato post-virale, nella sindrome di Kartergerner e in altre condizioni correlate;
- Alterazione del riflesso della tosse;
- Accumulo di secrezioni come si osserva nella fibrosi cistica o nell’ostruzione bronchiale.
Hai bisogno di un parere su questa condizione?

Dott.ssa Carmela Cilione
30 minuti - 75 € 33 anni di esperienza Area di Pneumologia Richiedi una televisita con: Dott.ssa Carmela CilioneGarantito in 24 ore! Con questo specialista o un suo collega.
Come si sviluppa la polmonite nel polmone :
Quando i germi superano le prime difese (vie aeree superiori) si possono annidare nel polmone ,vengono attivati I macrofagi (che fungono da “spazzini “ dei tessuti inglobando i germi e inattivandoli) e servono a proteggere il polmone da agenti patogeni.I macrofagi inghiottono questi agenti patogeni e attivano molecole segnale o citochine come TNF-a, IL-8 e IL-1 che reclutano cellule infiammatorie come i neutrofili nel sito dell’infezione.Il meccanismo che si attiva è causa dell’infiammazione del parenchima polmonare ciò rende i capillari di rivestimento “permeabili”, il che porta alla congestione essudativa.
Per il lettore non specialista è importante comprendere che, in sostanza, l’infezione attiva una risposta di difesa che “riempie” gli spazi d’aria del polmone con cellule infiammatorie e liquidi. È proprio questa combinazione di infezione e infiammazione a determinare i sintomi (febbre, tosse, fiato corto) e i reperti radiologici tipici della polmonite.
Classificazione delle polmoniti
Ci sono stati molti tentativi di classificare la polmonite in base all’eziologia, al contesto clinico in cui il paziente ha acquisito l’infezione e al tipo di coinvolgimento del parenchima polmonare.
Classificazione clinica: CAP, HAP e VAP
Riportiamo la classificazione seguita dall’American Thoracic Society.
- Polmonite acquisita in comunità (CAP): si tratta di qualsiasi polmonite acquisita al di fuori di un ospedale in un ambiente comunitario.
- Polmonite acquisita in ospedale (HAP): si tratta di qualsiasi polmonite acquisita 48 ore dopo che il paziente è stato ricoverato in un ambiente ospedaliero e non in incubazione al momento del ricovero.
- Polmonite associata al ventilatore (VAP): si tratta di qualsiasi polmonite acquisita 48 ore dopo l’intubazione endotracheale.
Questa suddivisione in categorie ha contribuito a stabilire gli organismi comuni responsabili di ciascun tipo di polmonite e ha contribuito a formulare linee guida di trattamento per una gestione efficiente sia in regime di ricovero che in regime ambulatoriale.
Classificazione morfologica: lobare, broncopolmonite, interstiziale
A seconda del modello di coinvolgimento, la polmonite è stata storicamente studiata anche come:
- Polmonite focale non segmentale o lobare: coinvolgimento di un singolo lobo del polmone;
- Broncopolmonite multifocale o polmonite lobulare;
- Polmonite interstiziale focale o diffusa.
Queste classificazioni descrivono il modo in cui l’infiammazione si distribuisce nel polmone. La polmonite lobare interessa un intero lobo, la broncopolmonite si presenta con più focolai disseminati e la polmonite interstiziale coinvolge soprattutto l’interstizio, cioè il tessuto che circonda gli alveoli. Queste informazioni sono particolarmente utili per radiologi e pneumologi nella lettura di radiografie e TAC e per in corretto inquadramento della patologia e il conseguente gisuto approccio terapeutico.
Polmonite lobare
La polmonite lobare è un consolidamento diffuso che coinvolge l’intero lobo del polmone. La sua evoluzione può essere suddivisa in 4 fasi come segue:
- Congestione: questa fase è caratterizzata da tessuto polmonare grossolanamente pesante e paludoso, congestione diffusa, congestione vascolare e accumulo di liquido alveolare ricco di organismi infettivi. In questa fase ci sono pochi globuli rossi (RBC) e neutrofili.
- Epatizzazione rossa: si osserva una marcata infiltrazione di globuli rossi, neutrofili e fibrina nel liquido alveolare. Grossolanamente, i polmoni appaiono rossi e sodi simili a un fegato, da qui il termine epatizzazione.
- Epatizzazione grigia: i globuli rossi si rompono e si formano essudati fibrinopurulenti che causano una trasformazione del colore da rosso a grigio.
- Risoluzione: caratterizzata dall’eliminazione degli essudati da parte dei macrofagi residenti con o senza formazione di tessuto cicatriziale residuo.
Broncopolmonite
La broncopolmonite è caratterizzata da un’infiammazione suppurativa localizzata in chiazze intorno ai bronchi che possono essere localizzate in un singolo lobo del polmone.
Molto raramente, forme gravi di polmonite possono provocare la formazione di ascessi polmonari, una completa rottura del tessuto e la formazione di sacche piene di pus nelle aree focali del polmone. Inoltre, l’infezione può diffondersi allo spazio pleurico formando un essudato fibrinopurulento che riempie questo spazio, noto come empiema.
Polmonite e broncopolmonite spesso possono complicarsi infettando a sua volta la pleura (foglietti che avvolgono il polmone) dando origine ad una pleurite associata.
Sintomi della polmonite
I sintomi della polmonite possono variare da forme lievi, simili a una semplice influenza, a quadri molto gravi che richiedono il ricovero urgente. In generale, la polmonite è caratterizzata da febbre, tosse e difficoltà respiratoria, con segni che possono cambiare in base all’età e alle condizioni di salute della persona.
Sintomi della polmonite negli adulti
Storicamente, i principali disturbi in caso di polmonite includono segni sistemici come febbre con brividi, malessere, perdita di appetito e mialgie. Questi sintomi sono più comuni nella polmonite virale rispetto alla polmonite batterica.
I reperti polmonari includono tosse con o senza produzione di espettorato. La polmonite batterica è associata a espettorato purulento o raramente macchiato di sangue. La polmonite virale è associata a produzione di espettorato acquoso o occasionalmente mucopurulento.
Può essere associato un dolore toracico pleurico con il concomitante coinvolgimento della pleura. Occasionalmente si osservano anche dispnea e una diffusa pesantezza del torace.
In pratica, nell’adulto i sintomi più frequenti della polmonite sono:
- tosse secca o produttiva (con catarro talvolta giallo-verde o striato di sangue);
- febbre, spesso accompagnata da brividi e sudorazione;
- fiato corto (dispnea), soprattutto sotto sforzo;
- dolore al petto che peggiora con il respiro profondo o col colpo di tosse;
- stanchezza marcata, senso di debolezza generale, perdita di appetito.
Non tutti questi segnali sono sempre presenti contemporaneamente e la loro intensità può essere molto diversa da persona a persona.
All’esame obiettivo solitamente si riscontra:
- Tachipnea
- Tachicardia
- Febbre con o senza brividi
- Suoni respiratori diminuiti
- Egofonia e fremito tattile, entrambi suggestivi di un processo di consolidamento
- Crepitii all’auscultazione delle regioni interessate del polmone
- Ottusità alle percussioni
Questi reperti vengono valutati dal medico durante la visita e non sono sempre percepibili dal paziente, ma aiutano a distinguere una polmonite da altre patologie respiratorie.
Sintomi della polmonite nei bambini
Nei bambini la polmonite può presentarsi in modo meno “classico” rispetto all’adulto e i sintomi possono essere più sfumati, soprattutto nei più piccoli. I segnali che devono destare attenzione includono:
- febbre, talvolta elevata o che non tende a ridursi con i comuni antipiretici;
- tosse secca o produttiva, che può peggiorare di notte;
- respiro rapido (tachipnea) o affannoso, con possibile rientramento delle costole o delle clavicole durante l’inspirazione;
- irritabilità, sonnolenza insolita o difficoltà a giocare come al solito;
- scarso appetito, difficoltà ad alimentarsi o a bere;
- nei lattanti, pianto inconsolabile, difficoltà a succhiare, possibile comparsa di cianosi (labbra o estremità bluastre).
Nei bambini più grandi il quadro può assomigliare di più a quello dell’adulto (febbre, tosse, dolore toracico e fiato corto), ma qualsiasi respiro insolitamente rapido o rumoroso va sempre segnalato al pediatra.
Sintomi della polmonite negli anziani e nei pazienti fragili
Negli anziani e nelle persone con patologie croniche (come malattie cardiache, broncopneumopatia cronica ostruttiva, diabete o immunodeficienze) la polmonite può manifestarsi con sintomi meno evidenti e meno “rumorosi”. Non sempre è presente febbre alta e talvolta la tosse può essere poco marcata.
Segnali frequenti in questa fascia di età includono:
- peggioramento improvviso della dispnea in un paziente con malattia respiratoria nota;
- confusione mentale, disorientamento o stato di agitazione acuta (“delirium”);
- cadute improvvise o marcata riduzione dell’autonomia rispetto ai giorni precedenti;
- stanchezza estrema, perdita di appetito, peggioramento delle condizioni generali senza causa apparente;
- febbre assente o solo modesta, ma con brividi, sudorazione o pallore.
In queste persone la polmonite ha un rischio maggiore di complicanze e di progressione rapida: la comparsa di respiro affannoso, confusione o peggioramento improvviso delle condizioni generali richiede sempre una valutazione urgente da parte del medico o in Pronto Soccorso.
Come si fa la diagnosi di polmonite
Per giungere alla diagnosi è necessario effettuare un’anamnesi approfondita e un accurato esame obiettivo. Molto importante è la valutazione radiologica.
Il medico raccoglie la storia dei sintomi (da quanto tempo sono presenti febbre e tosse, come si è modificato il respiro, eventuali patologie preesistenti), esegue l’auscultazione del torace con lo stetoscopio, valuta la frequenza respiratoria e cardiaca e, spesso, misura la saturazione di ossigeno con un saturimetro.
Secondo le linee guida della Infectious Diseases Society of America (IDSA) e dell’American Thoracic Society (ATS), il metodo migliore per la diagnosi di polmonite è la presenza di infiltrato alla radiografia del torace. I reperti possono variare da un infiltrato lobare a interstiziale, a lesioni occasionalmente cavitarie con livelli di aria-fluido suggestivi di un processo patologico più grave.
In molti casi, quindi, la conferma di polmonite richiede almeno una radiografia del torace. Nei quadri complessi o dubbi, il medico può richiedere una TAC del torace per valutare meglio l’estensione e le caratteristiche delle lesioni.
Gli esami di laboratorio includono una serie di test come emocoltura, coltura dell’espettorato e microscopia, emocromo di routine e conteggio dei linfociti. Per alcuni agenti patogeni possono essere utilizzati test speciali come il test dell’antigene urinario, l’aspirato bronchiale o l’espettorato indotto. Due test, la procalcitonina e la proteina C-reattiva aiutano a differenziare le cause virali da quelle batteriche quando i risultati clinici e radiologici potrebbero non essere evidenti.
Come si trattano le polmoniti
Il trattamento della polmonite dipende dal tipo di agente causale, dalla gravità dei sintomi e dalle condizioni generali del paziente. L’obiettivo è eliminare l’infezione, controllare i sintomi e prevenire le complicanze.
La gestione della CAP comporta la stratificazione iniziale del rischio del paziente e la decisione se gestire il paziente in regime ambulatoriale, in un reparto di medicina interna o in un’unità di terapia intensiva. Per questo scopo si usa la scala “CURB-65”
In parole semplici, esistono scale di gravità che aiutano il medico a decidere se la polmonite possa essere curata a casa o richieda il ricovero. Nelle forme lievi, il paziente viene trattato a domicilio con antibiotici (nel caso di sospetta origine batterica), riposo, idratazione e controlli clinici. Nelle forme più severe è necessario il ricovero, la somministrazione di antibiotici per via endovenosa e un monitoraggio più stretto dei parametri vitali.
La gestione delle VAP e HaP è conforme alle linee guida ATS/IDSA. È molto più complicata e comporta l’uso di antibiotici ad ampio spettro rispetto alla gestione della CAP.
Possibili complicanze e decorso della polmonite
Le complicanze della polmonite non trattata o sotto-trattata comprendono insufficienza respiratoria, sepsi, infezioni metastatiche, empiema, ascesso polmonare e disfunzione multiorgano.
Anche quando la terapia è adeguata, il recupero può richiedere tempo: la febbre tende a ridursi in pochi giorni, ma la stanchezza e la tosse possono persistere per settimane, soprattutto negli anziani o nei pazienti con patologie croniche. È importante seguire le indicazioni del medico, completare il ciclo di antibiotici prescritto e sottoporsi ai controlli raccomandati.
Consigli utili: quando rivolgersi al medico di medicina generale o al Pronto Soccorso
È consigliabile contattare il medico se:
- la febbre dura più di qualche giorno o si associa a tosse persistente;
- compaiono fiato corto, senso di oppressione o dolore al torace;
- i sintomi respiratori peggiorano nonostante una terapia già in corso;
- un bambino presenta respiro rapido, difficoltà ad alimentarsi o appare insolitamente sonnolento o irritabile.
Occorre rivolgersi con urgenza al Pronto Soccorso se si manifestano:
- respiro molto affannoso o difficoltà a parlare per la mancanza di fiato;
- confusione, disorientamento o perdita di coscienza;
- labbra o dita bluastre (cianosi);
- dolore toracico intenso o improvviso;
- febbre molto alta accompagnata da brividi, in particolare in anziani, bambini piccoli e persone con malattie croniche.
Hai bisogno di un parere su questa condizione?

Dott.ssa Carmela Cilione
30 minuti - 75 € 33 anni di esperienza Area di Pneumologia Richiedi una televisita con: Dott.ssa Carmela CilioneGarantito in 24 ore! Con questo specialista o un suo collega.
Bibliografia
- Mackenzie G. The definition and classification of pneumonia. Pneumonia (Nathan). 2016;8:14.
- Mandell LA, Wunderink RG, Anzueto A, Bartlett JG, Campbell GD, Dean NC, Dowell SF, File TM, Musher DM, Niederman MS, Torres A, Whitney CG., Infectious Diseases Society of America. American Thoracic Society. Infectious Diseases Society of America/American Thoracic Society consensus guidelines on the management of community-acquired pneumonia in adults. Clin Infect Dis. 2007 Mar 01;44 Suppl 2:S27-72.
- Kalil AC, Metersky ML, Klompas M, Muscedere J, Sweeney DA, Palmer LB, Napolitano LM, O’Grady NP, Bartlett JG, Carratalà J, El Solh AA, Ewig S, Fey PD, File TM, Restrepo MI, Roberts JA, Waterer GW, Cruse P, Knight SL, Brozek JL. Executive Summary: Management of Adults With Hospital-acquired and Ventilator-associated Pneumonia: 2016 Clinical Practice Guidelines by the Infectious Diseases Society of America and the American Thoracic Society. Clin Infect Dis. 2016 Sep 01;63(5):575-82.
- Canadian Critical Care Trials Group. A randomized trial of diagnostic techniques for ventilator-associated pneumonia. N Engl J Med. 2006 Dec 21;355(25):2619-30
- Gharib AM, Stern EJ. Radiology of pneumonia. Med Clin North Am. 2001 Nov;85(6):1461-91, x.
- Bartlett JG. Diagnostic tests for agents of community-acquired pneumonia. Clin Infect Dis. 2011 May;52 Suppl 4:S296-304.
- Sattar SBA, Sharma S. StatPearls [Internet]. StatPearls Publishing; Treasure Island (FL): Jun 15, 2021. Bacterial Pneumonia.
- Jain S, Self WH, Wunderink RG, Fakhran S, Balk R, Bramley AM, Reed C, Grijalva CG, Anderson EJ, Courtney DM, Chappell JD, Qi C, Hart EM, Carroll F, Trabue C, Donnelly HK, Williams DJ, Zhu Y, Arnold SR, Ampofo K, Waterer GW, Levine M, Lindstrom S, Winchell JM, Katz JM, Erdman D, Schneider E, Hicks LA, McCullers JA, Pavia AT, Edwards KM, Finelli L., CDC EPIC Study Team. Community-Acquired Pneumonia Requiring Hospitalization among U.S. Adults. N Engl J Med. 2015 Jul 30;373(5):415-27.
- Hage CA, Knox KS, Wheat LJ. Endemic mycoses: overlooked causes of community acquired pneumonia. Respir Med. 2012 Jun;106(6):769-76.
- Weiner LM, Webb AK, Limbago B, Dudeck MA, Patel J, Kallen AJ, Edwards JR, Sievert DM. Antimicrobial-Resistant Pathogens Associated With Healthcare-Associated Infections: Summary of Data Reported to the National Healthcare Safety Network at the Centers for Disease Control and Prevention, 2011-2014. Infect Control Hosp Epidemiol. 2016 Nov;37(11):1288-1301.
- Jones RN. Microbial etiologies of hospital-acquired bacterial pneumonia and ventilator-associated bacterial pneumonia. Clin Infect Dis. 2010 Aug 01;51 Suppl 1:S81-7.
- Ramirez JA, Wiemken TL, Peyrani P, Arnold FW, Kelley R, Mattingly WA, Nakamatsu R, Pena S, Guinn BE, Furmanek SP, Persaud AK, Raghuram A, Fernandez F, Beavin L, Bosson R, Fernandez-Botran R, Cavallazzi R, Bordon J, Valdivieso C, Schulte J, Carrico RM., University of Louisville Pneumonia Study Group. Adults Hospitalized With Pneumonia in the United States: Incidence, Epidemiology, and Mortality. Clin Infect Dis. 2017 Nov 13;65(11):1806-1812.
- Arnold FW, Wiemken TL, Peyrani P, Ramirez JA, Brock GN., CAPO authors. Mortality differences among hospitalized patients with community-acquired pneumonia in three world regions: results from the Community-Acquired Pneumonia Organization (CAPO) International Cohort Study. Respir Med. 2013 Jul;107(7):1101-11.
- Barbier F, Andremont A, Wolff M, Bouadma L. Hospital-acquired pneumonia and ventilator-associated pneumonia: recent advances in epidemiology and management. Curr Opin Pulm Med. 2013 May;19(3):216-28.
- Shorr AF, Zilberberg MD, Reichley R, Kan J, Hoban A, Hoffman J, Micek ST, Kollef MH. Validation of a clinical score for assessing the risk of resistant pathogens in patients with pneumonia presenting to the emergency department. Clin Infect Dis. 2012 Jan 15;54(2):193-8.
- Torres A, Niederman MS, Chastre J, Ewig S, Fernandez-Vandellos P, Hanberger H, Kollef M, Li Bassi G, Luna CM, Martin-Loeches I, Paiva JA, Read RC, Rigau D, Timsit JF, Welte T, Wunderink R. International ERS/ESICM/ESCMID/ALAT guidelines for the management of hospital-acquired pneumonia and ventilator-associated pneumonia: Guidelines for the management of hospital-acquired pneumonia (HAP)/ventilator-associated pneumonia (VAP) of the European Respiratory Society (ERS), European Society of Intensive Care Medicine (ESICM), European Society of Clinical Microbiology and Infectious Diseases (ESCMID) and Asociación Latinoamericana del Tórax (ALAT). Eur Respir J. 2017 Sep;50(3)
- Mbata GC, Chukwuka CJ, Onyedum CC, Onwubere BJ. The CURB-65 scoring system in severity assessment of Eastern Nigerian patients with community-acquired pneumonia: a prospective observational study. Prim Care Respir J. 2013 Jun;22(2):175-80.
- Castro-Guardiola A, Armengou-Arxé A, Viejo-Rodríguez A, Peñarroja-Matutano G, Garcia-Bragado F. Differential diagnosis between community-acquired pneumonia and non-pneumonia diseases of the chest in the emergency ward. Eur J Intern Med. 2000 Dec 20;11(6):334-339.
Categorie
- Allergie e intolleranze
- Apparato Urogenitale
- Autismo e Disturbi dello Spettro Autistico
- Benessere Psichico e Salute mentale
- Caduta dei Capelli
- Coronavirus
- Disfunzioni della Tiroide
- Disturbi Alimentari
- Disturbi del Sonno
- Disturbi Gastrointestinali
- Epidemie e pandemie
- Farmaci - Terapie - effetti collaterali
- Malattie Autoimmuni
- Malattie infettive
- Malattie Infiammatorie
- malattie renali
- Malattie Respiratorie
- Malattie Reumatiche
- News
- Patologie Cardiovascolari
- Patologie del Piede
- Patologie del Sangue e della Coagulazione
- Patologie del Sistema Nervoso
- Patologie della Pelle
- Patologie Oculari
- Prevenzione e salute
- Problemi Muscoloscheletrici
- Salute dei Bambini
- Salute dell'Anziano
- Salute della Donna
- Sessualità e coppia
- Telemedicina
- Terapie e Rimedi Naturali
- Terapie Oncologiche
- Viaggi e Salute
- Video
- Vivere con il Diabete






